Tipos de vacunas: ¿qué tecnología se emplea para cada una?
Son varios los tipos de vacunas que existen, para desarrollar una frente al SARS-CoV-2 se utilizan diversas plataformas de vacunas:1
-
Vacunas con virus vivos atenuados y con virus inactivados.
-
Vacunas con subunidades proteicas.
-
Vacunas de ácido nucleico (ARNm).
-
Vacunas con vectores víricos replicativos y no replicativos.
Cada una de ellas actúa de una manera diferente para generar una respuesta inmunitaria o generar antígenos en nuestro organismo y cada tecnología empleada tiene ventajas e inconvenientes que deben tenerse en cuenta a la hora de desarrollar una vacuna frente a la COVID-192.
Algunas de las plataformas llevan tiempo utilizándose para otros virus y bacterias y están consolidadas (vacunas con virus inactivados, vacunas con subunidades proteicas), mientras otras son más modernas (vacunas de ARNm, vacunas con vectores víricos)3.
La mayoría de vacunas frente a la COVID-19 que se están desarrollando se dirigen a la proteína S del SARS-CoV-2 como antígeno2,3.
¿Qué tipos de vacunas existen?: descripción, ventajas e inconvenientes
Vacunas de virus inactivados o atenuados
Se trata de unas vacunas de virus completo, se utiliza todo el virus para inducir la respuesta inmunitaria. Los virus pueden haberse inactivado o estar vivos y atenuados2.
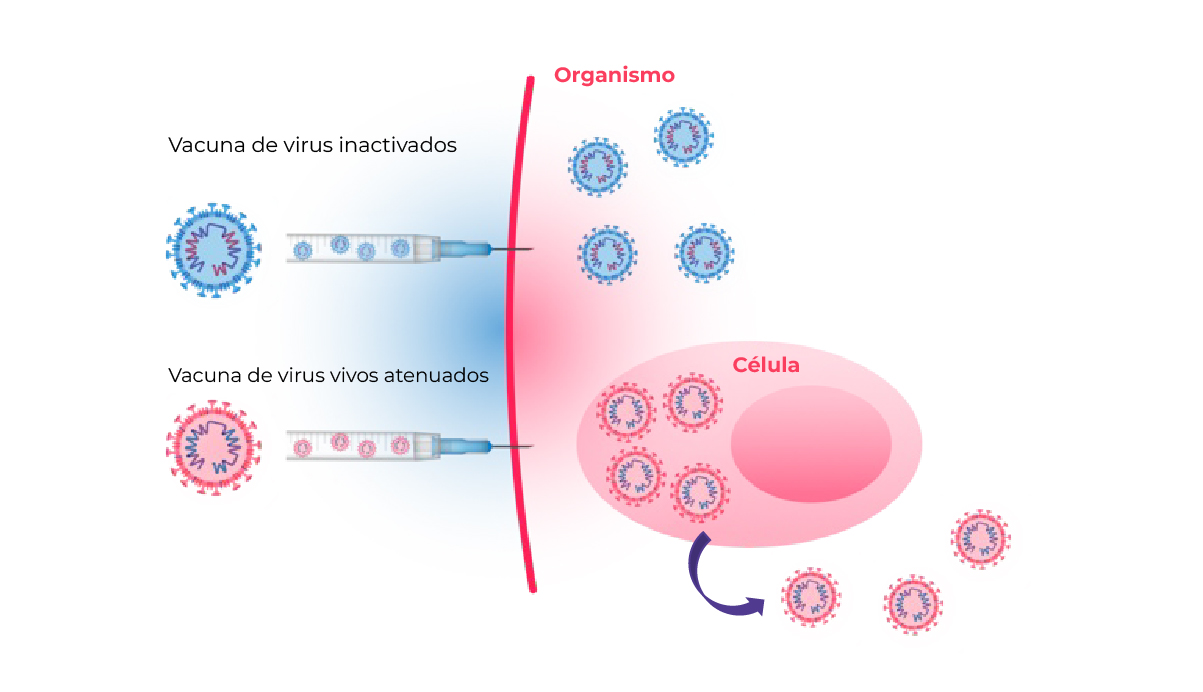
Creado a partir de Callaway et al. 2020.
Al inyectar una vacuna con virus inactivados, estos no se replican. Por otro lado, al inyectar una vacuna con virus vivos atenuados, la multiplicación de los virus en las células es escasa. En ambos casos la vacuna induce una respuesta inmunitaria protectora4.
Vacunas con virus inactivados
Las vacunas con virus inactivados se producen al cultivar el virus en laboratorio e inactivarlo con calor o productos químicos. Estos virus no pueden replicarse, por lo que no causan la enfermedad5 y los pacientes están expuestos a todos los antígenos de superficie del virus2-4.
La respuesta inmunitaria a la vacuna inactivada es principalmente humoral, es decir, a base de anticuerpos5 y acostumbran a necesitar varias dosis5.
|
Posibles ventajas* |
|
|
Posibles limitaciones* |
|
Creado a partir de Funk et al. 20206.
* Hace referencia a las características generales de estas plataformas y no predice las características futuras de las posibles vacunas.
Vacunas con virus vivos atenuados
Los virus vivos atenuados proceden de virus aislados a partir de muestras clínicas que se atenúan (debilitan) en el laboratorio con el fin de mermar su capacidad de infección y replicación2,3,5.
Estos virus se replican lo suficiente en la persona vacunada como para inducir una respuesta inmunitaria pero, la enfermedad no suele darse en el mismo grado que podría provocar el virus natural. Por tanto, replica los resultados que produce una infección natural5.
A menudo, las vacunas con virus vivos atenuados son capaces de producir inmunidad tras una única dosis5.
|
Posibles ventajas* |
|
|
Posibles limitaciones* |
|
Creado a partir de Funk et al. 20206.
* Hace referencia a las características generales de estas plataformas y no predice las características futuras de las posibles vacunas.
Acceda aquí a las recomendaciones sanitarias y de salud pública de interés general del Ministerio de Sanidad sobre la COVID-19
Vacunas con subunidades proteicas
Las vacunas con subunidades proteicas o vacunas recombinantes se crean al producir una proteína vírica in vitro5.
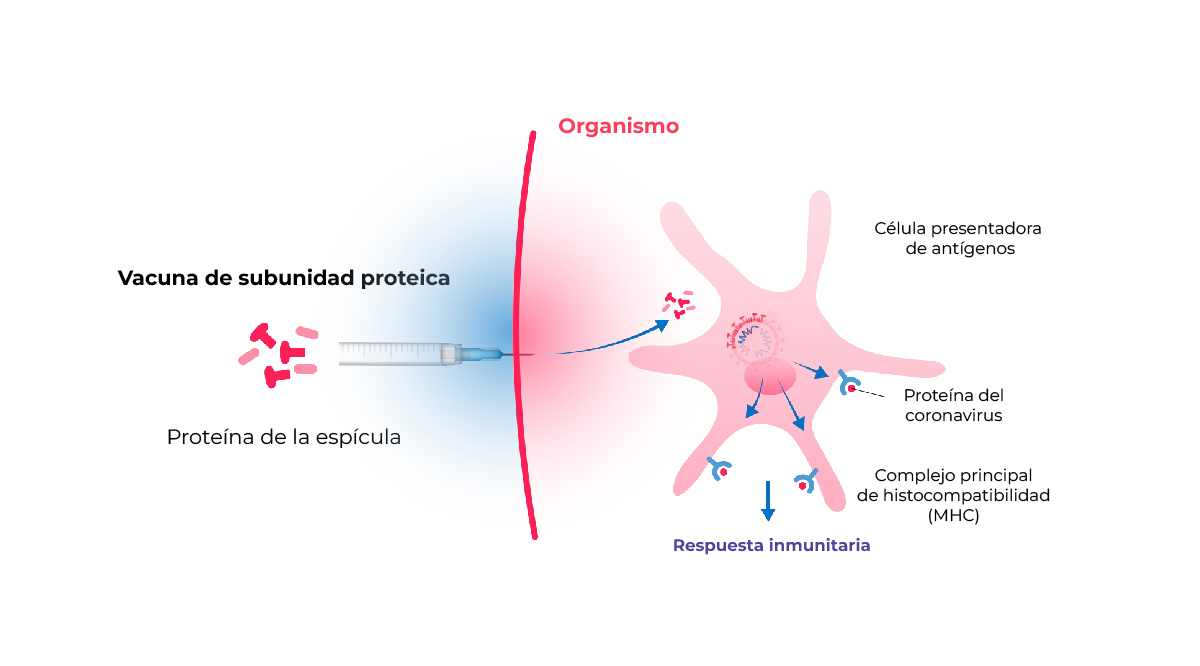
Creado a partir de Callaway et al. 2020.
Cuando se inyecta una vacuna con subunidades proteicas víricas, las células presentadoras de antígenos las capturan y activan una respuesta inmunitaria protectora7.
Al no contener el virus completo, estas vacunas no presentan riesgo de causar la enfermedad. Pero, requieren varias dosis.
|
Posibles ventajas* |
|
|
Posibles limitaciones* |
|
Creado a partir de Funk et al. 20206.
* Hace referencia a las características generales de estas plataformas y no predice las características futuras de las posibles vacunas.
Acceda aquí a las recomendaciones sanitarias y de salud pública de interés general del Ministerio de Sanidad sobre la COVID-19
Vacunas de ácido nucleico (ARN mensajero)
Actualmente, hay varias vacunas de ácido nucleico frente a la COVID-19 en fase de ensayos clínicos8.
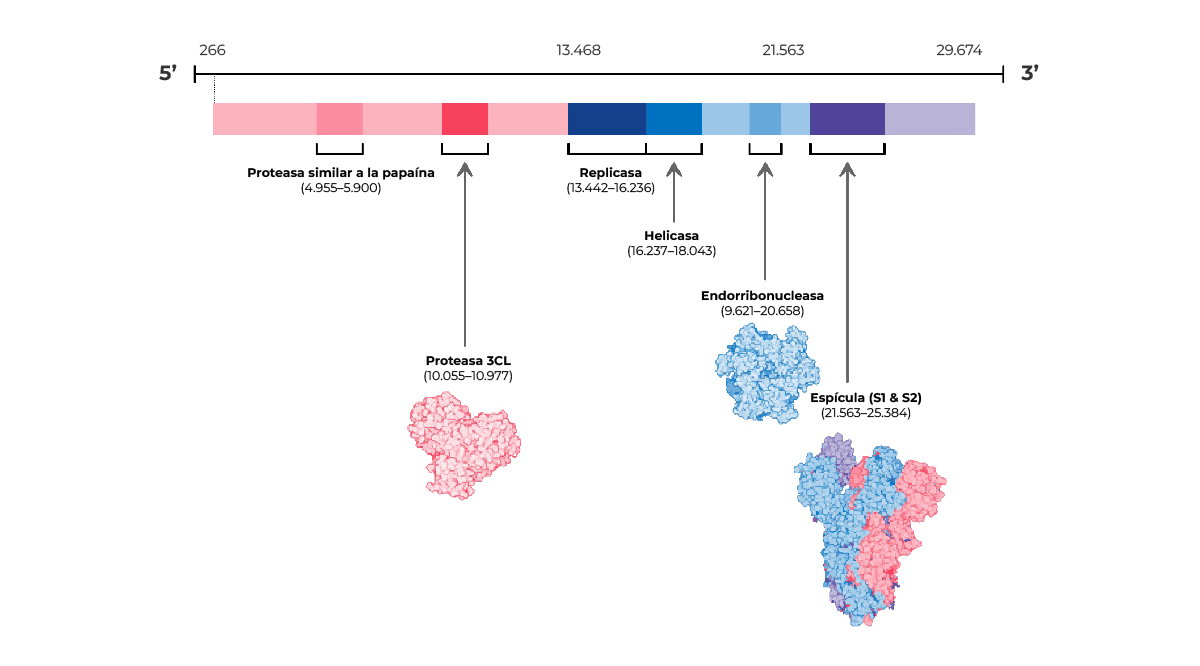
Creado a partir de Cascella et al. 2020.
El objetivo de estas vacunas es transferir el material genético que codifica un antígeno del SARS-CoV-2 a una célula diana, que actuará como “fábrica” para producir el antígeno vírico1.
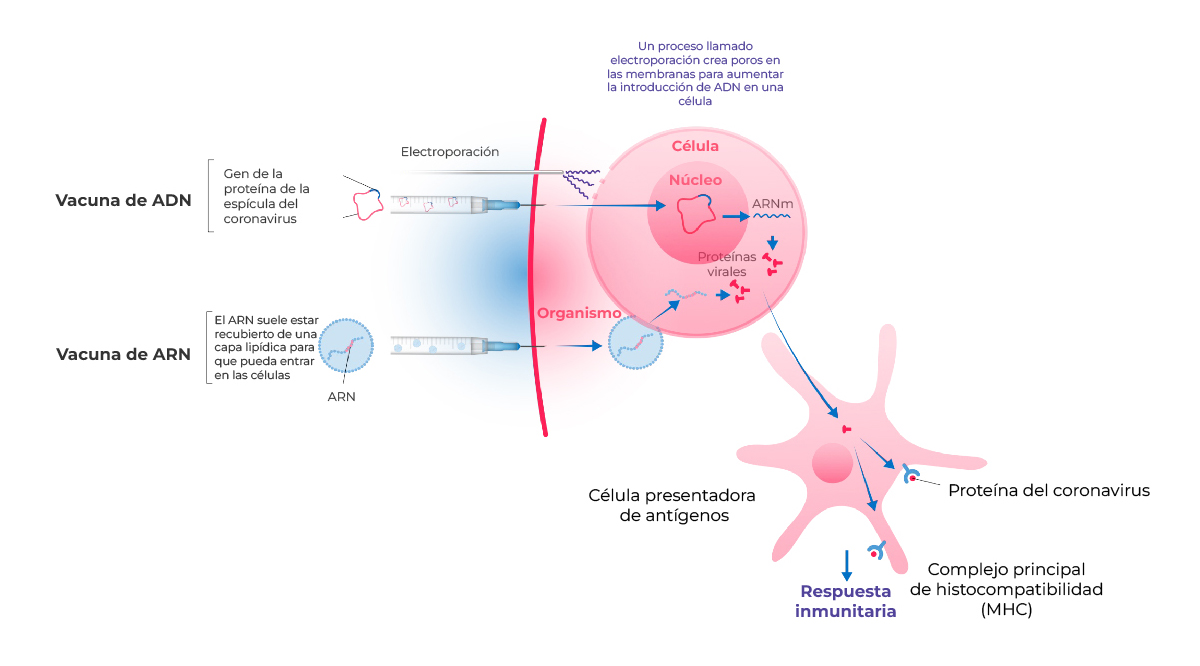
Creado a partir de Cascella et al. 2020.
Las vacunas de ARNm se clasifican en dos grandes grupos:
-
Las vacunas de ARNm no replicativo (NRM, non-replicating mRNA) contienen la secuencia que codifica el antígeno vírico11.
-
Las vacunas de ARNm autoamplificado (SAM, self-amplifying mRNA) contienen regiones que codifican las proteínas que intervienen en la replicación del ARNm, además de la secuencia codificadora del antígeno vírico. Esto permite que la célula diana pueda replicar varias veces una pequeña dosis de ARNm y potenciar la expresión de los antígenos11.
|
Posibles ventajas* |
|
|
Posibles limitaciones* |
|
Creado a partir de Funk et al. 20206.
* Hace referencia a las características generales de estas plataformas y no predice las características futuras de las posibles vacunas.
El desarrollo de vacunas de ARNm se hahabía visto frenado por la inestabilidad de estas moléculas y por su elevada sensibilidad a un tipo de enzimas extracelulares llamadas ribonucleasas (o ARNsas), que rompen y degradan el ARNm12.
Sin embargo, durante la última década, destacadas innovaciones tecnológicas e inversiones en materia de investigación han propiciado que los ARNm pasen a ser una prometedora herramienta terapéutica por su potencial como plataforma de vacunas13.
Acceda aquí a las recomendaciones sanitarias y de salud pública de interés general del Ministerio de Sanidad sobre la COVID-19
Vacunas con vectores víricos replicativos y no replicativos
Varias posibles vacunas con vectores víricos frente a la COVID-19 se encontraban en fase de ensayos clínicos8.
Estas vacunas se parecen a las de ácido nucleico, ya que transfieren el material genético de un antígeno del SARS-CoV-2 (normalmente la proteína S) a una célula diana, que actuará como “fábrica” para producir el antígeno1 (véase la figura siguiente).
Sin embargo, en vez de utilizar un sistema de transferencia como la encapsulación en una nanopartícula lipídica, se basan en un virus modificado no emparentado (es decir, que no es un coronavirus) para transferir el gen a las células diana2.
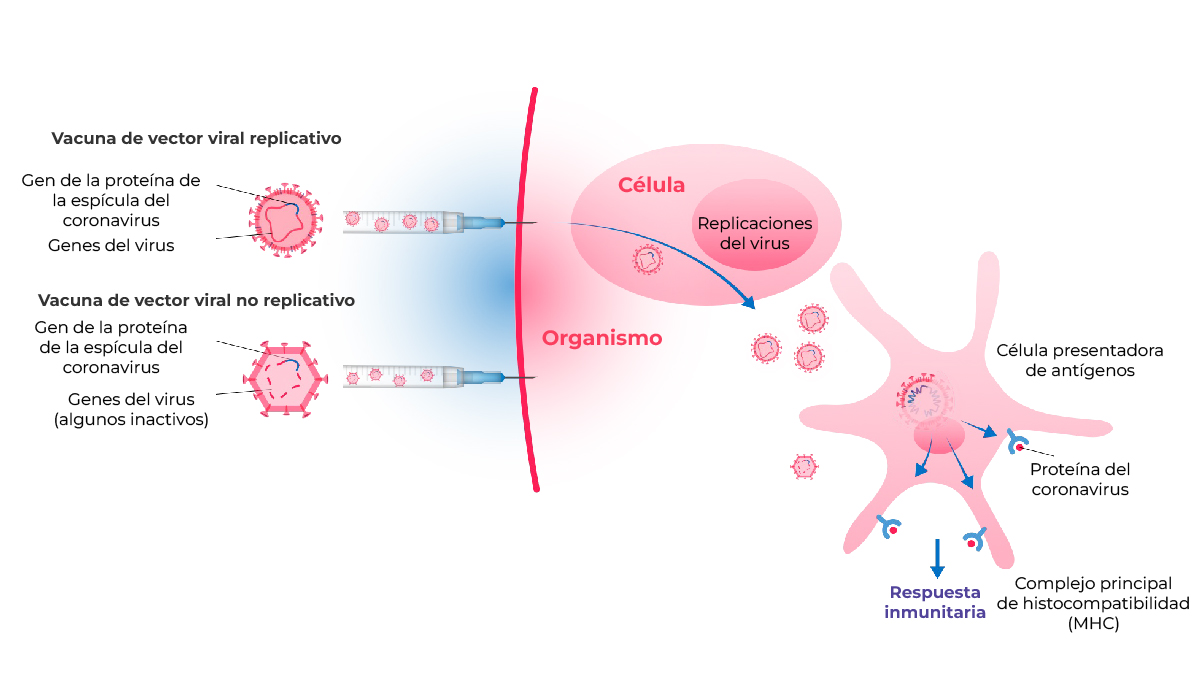
Creado a partir de Callaway et al. 2020
Cuando se inyecta una vacuna con vector vírico replicativo, los virus «vectores» se replican en las células hospedadoras. Cuando se inyecta una vacuna con vector vírico no replicativo, los virus «vectores» no se multiplican, porque algunos de sus genes han sido inactivados14.
Uno de los vectores utilizados en las plataformas de vacunas con vectores víricos es el adenovirus, un virus común que posee un genoma de ADN y que suele asociarse a enfermedades infantiles de las vías respiratorias superiores, entre ellas el resfriado común15. Los vectores adenovíricos pueden desencadenar potentes respuestas inmunitarias humorales y celulares.
La utilización de estos vectores en humanos se ve limitada por la frecuencia de estos virus en el hombre, ya que muchas personas presentan inmunidad preexistente a estos virus16.
|
Posibles ventajas* |
|
|
Posibles limitaciones* |
|
Creado a partir de Funk et al. 20206.
* Hace referencia a las características generales de estas plataformas y no predice las características futuras de las posibles vacunas.
Acceda aquí a las recomendaciones sanitarias y de salud pública de interés general del Ministerio de Sanidad sobre la COVID-19
PP-CMR-ESP-0232
Bibliografía
-
AEMPS. ¿cómo funcionan las vacunas? https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca… Último acceso: septiembre de 2024
-
Callaway E. The race for coronavirus vaccines. Nature. 2020;580:576-577.
-
OMS. Los distintos tipos de vacunas que existen. Los distintos tipos de vacunas que existen (who.int) Último acceso: septiembre de 2024
-
History of Vaccines. Diferentes tipos de vacunas. https://historyofvaccines.org/vaccines-101/what-do-vaccines-do/diferent… Último acceso: septiembre de 2024
-
United States Centers for Disease Control and Prevention. Chapter 1: Principles of Vaccination. https://www.cdc.gov/vaccines/pubs/pinkbook/prinvac.html. Último acceso: septiembre de 2024
-
Funk CD, Laferriere C, Ardakani A. A snapshot of the global race for vaccines targeting SARS-CoV-2 and the COVID-19 pandemic. Front Pharmacol. 2020;11:1-17.
-
Plotkin, S.A., Orenstein, W.A., Offit, P.A., eds. Vaccines, 6th ed. Philadelphia: Elsevier; 2013
-
COVID-NMA. COVID-19 open living evidence synthesis to inform decision. https://covid-nma.com/vaccines/mapping/. Último acceso: septiembre de 2024
-
Clancy S, Brown W. Translation: mRNA to protein. Nature Education. 2008;1;101.
-
Cascella M, Rajnik M, Cuomo A, et al. Features, evaluation, and treatment of coronavirus (COVID-19). https://pubmed.ncbi.nlm.nih.gov/32150360/. Último acceso: septiembre de 2024
-
Jackson NAC, Kester KE, Casimiro D, et al. The promise of mRNA vaccines: A biotech and industrial perspective. NPJ Vaccines. 2020;5:1-6.
-
Okay S, Ozcan OO, Karahan M. Nanoplarticle-based delivery platforms for mRNA vaccine development. AIMS Biophysics. 2020;7:323-33.
-
Pardi N, Hogan MJ, Porter FW, et al. mRNA vaccines – a new era in vaccinology. Nat Rev Drug Discov. 2018;17:261-279.
-
United States Centers for Disease Control and Prevention. Información sobre cómo actúan las vacunas de vectores virales contra el COVID-19. https://espanol.cdc.gov/coronavirus/2019-ncov/vaccines/different-vaccin…. Último acceso: septiembre de 2024
-
Khanal S, Ghimire P, Dhamoon AS. The repertoire of adenovirus in human disease: The innocuous to the deadly. Biomedicines. 1028;6:1-12.
-
Rauch S, Jasny E, Schmitdt KE, et al. New vaccione technologies to combat outbreak situations. Front Immunol. 2020;9:1-24.
-
Folegatti PM, Ewer KJ, Aley PK, et al. Safety and immunogenecity of the ChAdOx1 nCoV-19 vaccione againts SARS-CoV-2: A preliminary report of a phase 1/2, single-blind, randomized controlled trial. Lancet. 2020. 1-13.
-
Zhu F-C, Guan X-H, Li Y-H, et al. Immunogenecity and safety of a recombinant adenovirus type-5-vectored COVID-19 vaccine in healthy adults aged 18 years or older: a rondomised, double-blind, placebo controlled, phase 2 trial. Lancet. 2020. 1-10.